
Đánh giá rủi ro như một công cụ đảm bảo quy trình chất lượng
-
Hãng sản xuất: Particle Measuring Systems - Mỹ Model: Document: -
Liên hệ
Đánh giá rủi ro là quá trình xác định mối nguy, phân tích khả năng xảy ra, đánh giá mức độ ảnh hưởng và lựa chọn biện pháp kiểm soát phù hợp. Trong sản xuất dược phẩm, rủi ro có thể xuất hiện ở nhiều điểm: nguyên liệu, thiết bị, con người, môi trường, quy trình vệ sinh, hệ thống HVAC, thao tác vận hành, dữ liệu giám sát và chương trình hiệu chuẩn.
Với sản xuất vô trùng, đánh giá rủi ro càng quan trọng vì các yếu tố như tiểu phân, vi sinh, luồng khí, áp suất chênh lệch, điểm lấy mẫu, tần suất giám sát và dữ liệu cảnh báo đều có thể ảnh hưởng trực tiếp đến khả năng kiểm soát nhiễm bẩn.
Quản lý rủi ro chất lượng giúp doanh nghiệp đưa ra quyết định dựa trên dữ liệu, kinh nghiệm vận hành và hiểu biết khoa học về quy trình. Thay vì chỉ phản ứng khi có sai lệch, nhà máy có thể chủ động nhận diện điểm yếu, ưu tiên nguồn lực và kiểm soát các yếu tố có khả năng ảnh hưởng đến chất lượng sản phẩm.
Trong sản xuất vô trùng, chiến lược kiểm soát nhiễm bẩn cần dựa trên hiểu biết đầy đủ về quy trình và rủi ro. Đánh giá rủi ro giúp xác định khu vực nào cần giám sát liên tục, điểm nào cần lấy mẫu định kỳ, thiết bị nào cần hiệu chuẩn chặt chẽ và dữ liệu nào cần được xem xét thường xuyên.
Ví dụ, nếu một khu vực có thao tác mở, sản phẩm tiếp xúc với môi trường hoặc nhân sự can thiệp thường xuyên, rủi ro nhiễm bẩn sẽ cao hơn khu vực kín. Khi đó, nhà máy có thể cần tăng cường giám sát tiểu phân, lấy mẫu vi sinh, kiểm soát luồng khí, kiểm soát áp suất và đánh giá lại tần suất vệ sinh.
Đánh giá rủi ro sẽ không đủ mạnh nếu thiếu dữ liệu đáng tin cậy. Trong phòng sạch dược phẩm, dữ liệu từ máy đếm tiểu phân, thiết bị lấy mẫu vi sinh, hệ thống giám sát online, sensor áp suất, nhiệt độ, độ ẩm và phần mềm quản lý dữ liệu giúp QA/QC hiểu rõ trạng thái thực tế của khu vực sản xuất.
Risk assessment is an important part of pharmaceutical quality systems, especially in sterile manufacturing, contamination control, cleanroom monitoring and environmental monitoring programs.
SAO NAM supports pharmaceutical manufacturers with Particle Measuring Systems equipment, airborne particle counters, microbial air samplers, online monitoring systems, calibration, repair and technical services in Vietnam.
For consultation on cleanroom monitoring, PMS equipment, calibration or contamination control solutions, please contact SAO NAM via hotline, Zalo or email.
Kiểm soát ô nhiễm phòng sạch
Máy đếm tiểu phân Lasair Pro
IsoAir Pro Plus - Giám sát tiểu phân online
Airnet 510 - Sensor đếm tiểu phân online
MiniCapt Remote - Máy lấy mẫu vi sinh online
Hiệu chuẩn thiết bị Particle Measuring Systems
Sửa chữa thiết bị PMS
Audit Trail trong hệ thống giám sát
- ICH Q9: Quality Risk Management
- EU GMP Annex 1: Manufacture of Sterile Medicinal Products
- Particle Measuring Systems: Risk Assessment as a Process Quality Assurance Tool
- ISO 14644: Cleanrooms and associated controlled environments

Đánh giá rủi ro như một công cụ đảm bảo quy trình chất lượng
Kiểm soát ô nhiễm môi trường là một thành phần quan trọng của sản xuất dược phẩm vô trùng và Quản lý Rủi ro là cần thiết để đảm bảo rằng các phương pháp kiểm soát phù hợp được áp dụng.
Đánh giá rủi ro định tính này có thể được chuyển đổi thành đánh giá định lượng bằng cách sử dụng các công cụ và quy trình phân tích rủi ro hiện đại; những công cụ này cung cấp cơ sở lý luận được lập thành văn bản đầy đủ .
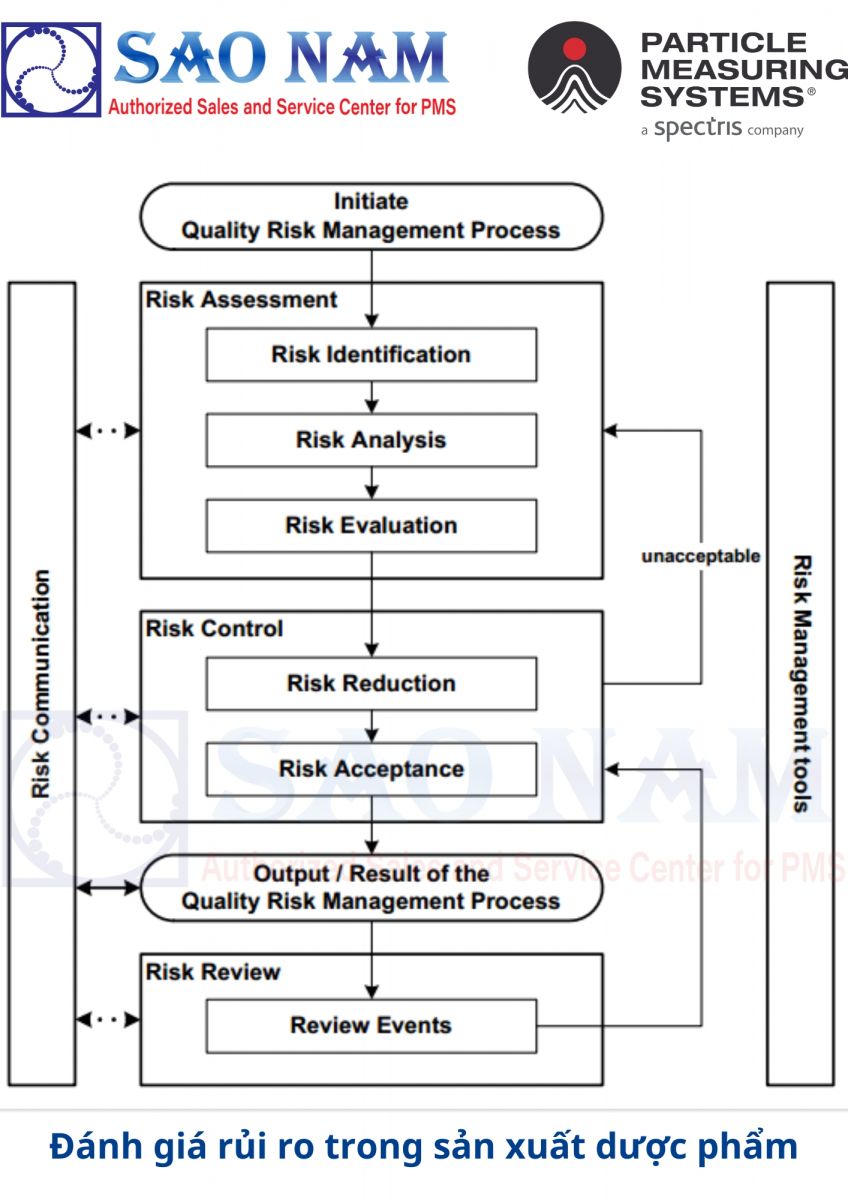
I-Khái niệm về rủi ro trong sản xuất dược phẩm
Trong sản xuất dược phẩm, rủi ro được hiểu là khả năng xảy ra các sự cố, sai sót hoặc hậu quả không mong muốn có thể ảnh hưởng đến chất lượng, an toàn hoặc hiệu quả của quy trình sản xuất và sản phẩm cuối cùng. Rủi ro trong ngành dược phẩm có thể bao gồm các vấn đề như:
-
1-Rủi ro liên quan đến chất lượng: Bao gồm khả năng xảy ra sai sót trong quy trình sản xuất, sử dụng nguyên liệu không đạt chất lượng, sai sót trong quá trình kiểm tra chất lượng, v.v. Điều này có thể dẫn đến sản phẩm không đạt yêu cầu chất lượng hoặc không an toàn cho sức khỏe của người dùng.
-
2-Rủi ro liên quan đến an toàn: Bao gồm khả năng xảy ra sự cố trong quy trình sản xuất có thể gây ra nguy hiểm cho nhân viên, như tai nạn lao động, tiếp xúc với chất độc hại, v.v. Rủi ro an toàn cũng liên quan đến khả năng sản phẩm gây ra tác động không mong muốn cho người dùng, như phản ứng phụ nghiêm trọng hoặc tác dụng phụ nghiêm trọng.
-
3-Rủi ro liên quan đến tuân thủ quy định: Bao gồm khả năng vi phạm các quy định pháp luật, quy trình, tiêu chuẩn và hướng dẫn của ngành dược phẩm. Vi phạm này có thể dẫn đến sự truy cứu pháp lý, phạt tiền, mất uy tín và rủi ro về hình ảnh cho công ty.
Để quản lý rủi ro trong sản xuất dược phẩm, các công ty thường thực hiện đánh giá rủi ro, xác định các biện pháp kiểm soát rủi ro, theo dõi và đánh giá hiệu quả của các biện pháp này. Điều này giúp đảm bảo rằng sản xuất dược phẩm được thực hiện theo các tiêu chuẩn cao nhất về chất lượng, an toàn và tuân thủ quy định.
II-Tại sao quản lý rủi ro lại quan trọng?
Trong dự thảo đã phát hành của EU GMP Phụ lục 1, Bản sửa đổi 12, tầm quan trọng của quản lý rủi ro được nhấn mạnh như một công cụ thích hợp để đảm bảo chất lượng của một quy trình.
Đây là một phần quan trọng của hệ thống quản lý chất lượng và được xem là tiêu chuẩn quốc tế trong ngành dược phẩm.
.jpg)
Quản lý rủi ro trong sản xuất dược phẩm là rất quan trọng vì một số lý do sau:
1-Đảm bảo chất lượng sản phẩm: Quản lý rủi ro giúp xác định và giảm thiểu các rủi ro tiềm ẩn có thể ảnh hưởng đến chất lượng của sản phẩm dược phẩm. Bằng cách tiếp cận rủi ro một cách chủ động, các công ty dược phẩm có thể duy trì chất lượng sản phẩm nhất quán trong suốt quá trình phát triển và sản xuất.
2-Đảm bảo an toàn cho bệnh nhân: Quản lý rủi ro đóng vai trò quan trọng trong việc đảm bảo an toàn cho bệnh nhân sử dụng các sản phẩm dược phẩm. Bằng cách xác định và giải quyết các rủi ro liên quan đến quy trình sản xuất, các công ty có thể giảm thiểu nguy cơ gây hại hoặc tác động tiêu cực đến bệnh nhân.
3-Tuân thủ quy định: Các cơ quan quản lý yêu cầu các công ty dược phẩm có quy trình quản lý rủi ro mạnh mẽ. Tuân thủ các hướng dẫn và yêu cầu của cơ quan quản lý là rất quan trọng để có được và duy trì các giấy phép và chứng chỉ cần thiết cho các sản phẩm dược phẩm.
4-Uy tín và sự tin tưởng: Quản lý rủi ro hiệu quả giúp bảo vệ uy tín của các công ty dược phẩm. Bằng cách thể hiện cam kết với chất lượng và an toàn của bệnh nhân thông qua các biện pháp quản lý rủi ro, các công ty có thể xây dựng sự tin tưởng với các chuyên gia y tế, bệnh nhân và cơ quan quản lý.
5-Giảm chi phí: Xác định và giải quyết rủi ro sớm trong quá trình sản xuất có thể giúp ngăn chặn các vấn đề về chất lượng, thu hồi sản phẩm và vi phạm quy định gây tốn kém. Bằng cách quản lý rủi ro một cách chủ động, các công ty có thể giảm thiểu tổn thất tài chính liên quan đến việc sản phẩm thất bại hoặc xảy ra sự cố an toàn.
Rõ ràng, quản lý rủi ro trong sản xuất dược phẩm là rất quan trọng để duy trì chất lượng sản phẩm, đảm bảo an toàn cho bệnh nhân, tuân thủ quy định, bảo vệ uy tín và giảm chi phí. Đây là một yếu tố quan trọng trong quá trình đảm bảo chất lượng trong ngành dược phẩm.
III-Quy trình quản lý rủi ro trong EU GMP
Quản lý rủi ro trong EU GMP đề cập đến việc xác định, đánh giá và kiểm soát các rủi ro có thể ảnh hưởng đến chất lượng sản phẩm. Các công ty dược phẩm cần thực hiện đánh giá rủi ro thường xuyên và liên tục trong toàn bộ quy trình sản xuất, từ nguyên liệu đến sản phẩm cuối cùng.
Quản lý rủi ro trong EU GMP đảm bảo rằng các công ty dược phẩm thực hiện các biện pháp để giảm thiểu rủi ro liên quan đến chất lượng, an toàn và tuân thủ quy định. Điều này đảm bảo rằng sản phẩm dược phẩm đáp ứng các tiêu chuẩn cao nhất và an toàn cho người dùng. Cụ thể gồm các bước:
Quá trình đánh giá rủi ro bao gồm các bước sau:
1-Xác định rủi ro: Bước đầu tiên là xác định các nguồn gốc tiềm ẩn gây hại (rủi ro) trong quá trình sản xuất dược phẩm. Điều này có thể được thực hiện thông qua việc sử dụng thông tin lịch sử, phân tích lý thuyết, ý kiến thông tin, các phiên họp ý tưởng, v.v. Mục tiêu là để có được cái nhìn sâu hơn về quá trình sản xuất
2-Phân tích rủi ro: Bước này liên quan đến ước lượng rủi ro liên quan đến các nguồn gốc đã xác định.
Đây là quá trình định tính hoặc định lượng liên kết giữa xác suất và mức độ nghiêm trọng của hại (mức độ nghiêm trọng là một đánh giá về hậu quả có thể xảy ra do một rủi ro) bằng cách đánh giá các biện pháp thiết kế/các biện pháp kiểm soát có khả năng kiểm soát sự xảy ra và phát hiện của chúng.
Phân tích mức độ rủi ro dẫn đến việc xác định các công cụ hoặc biện pháp phù hợp để quản lý rủi ro theo thời gian.
Một số công cụ quản lý rủi ro cũng có thể xem xét khả năng phát hiện hại (khả năng phát hiện) như một yếu tố ảnh hưởng đến đánh giá tổng thể về rủi ro.
3-Đánh giá rủi ro: Bước này liên quan đến việc so sánh mức độ rủi ro được ước tính với các tiêu chí rủi ro nhất định. Điều này được thực hiện thông qua việc sử dụng một thang đo để xác định sự quan trọng của rủi ro và sau đó đặt một ngưỡng chấp nhận được. Khi rủi ro được biểu thị bằng cách định lượng, ta sử dụng xác suất số học. Ngoài ra, rủi ro cũng có thể được biểu thị bằng cách sử dụng các mô tả định tính như "cao", "trung bình" hoặc "thấp", tuy nhiên, nên được định nghĩa càng chi tiết càng tốt. Mục tiêu của quản lý rủi ro là giảm rủi ro xuống một mức chấp nhận được, được xác định trước.
IV-Các phương pháp để phân tích rủi ro
Có một số phương pháp khoa học hiện có để phân tích rủi ro, và chúng có thể được sử dụng độc lập hoặc kết hợp để đạt được kết quả tốt nhất. Ví dụ, việc kết hợp phương pháp HACCP với FMEA có thể tạo ra các tài liệu toàn diện hơn. Dưới đây là ba phương pháp quan trọng:
-
1.HACCP: Phương pháp tiếp cận HACCP là một công cụ hệ thống, chủ động và phòng ngừa để đảm bảo chất lượng, độ tin cậy và an toàn. Dựa trên việc phát triển cây quyết định, phương pháp này giúp xác định các lĩnh vực quan trọng và không quan trọng của quy trình được phân tích.
-
2.FMEA: Phương pháp FMEA (Failure Mode and Effects Analysis) được sử dụng để xác định và đánh giá các lỗi tiềm ẩn và tác động của chúng đến quy trình sản xuất. Bằng cách xác định các yếu tố gây rủi ro và ưu tiên các biện pháp kiểm soát, FMEA giúp giảm thiểu rủi ro và cải thiện chất lượng sản phẩm.
-
3.Risk Assessment: Đánh giá rủi ro là một phương pháp quan trọng để xác định và đánh giá các rủi ro trong quy trình sản xuất dược phẩm. Bằng cách sử dụng các công cụ và phương pháp như phân tích nguy cơ, đánh giá tác động và xác định nguy cơ, công ty có thể xác định các rủi ro tiềm ẩn và triển khai các biện pháp kiểm soát phù hợp.
Đọc và lấy tài liệu miễn phí tại link sau https://www.pmeasuring.com/application_note/317-risk-assessment-as-a-process-quality-assurance-tool/
LIÊN HỆ CHÚNG TÔI NGAY ĐỂ NHẬN NGAY TÀI LIỆU
VP chính : 92 Đường 13, Phường Bình Trị Đông B, Quận Bình Tân, TP.HCM
Hotline : (84.28) 6260 2704 / 0903938641 – Email : info@saonamchem.com
Website : https://www.saonamchem.com https://www.saonam.vn hoặc https://www.pmsvietnam.vn
Nguồn tham khảo
[1] EudraLex - Volume 4 - Good Manufacturing Practice (GMP) guidelines – Annex I
[2] ICH Q9 Quality risk management
[3] art. 2, lettera s, D. Lgs. 81/08
[4] ISO/IEC Guide 51:1999 - Safety Aspects - Guideline for their inclusion in standards
[5] ICH Q6A
[6] The Basics of FMEA, Robin McDermott, Raymond J. Mikulak, Michael R. Beauregard 1996, ISBN 0527763209.
[7] WHO Technical Report Series No 908, 2003 Annex 7
#risk #quality #pharmaceuticalmanufacturing #riskmanagement #annex1
- Cam kết chất lượng
- Bảo hành chính hãng
- Giao hàng tận nơi
- DỊCH VỤ 24/7
 SAO NAM - Đại lý & Trung tâm dịch vụ Particle Measuring Systems tại Việt Nam
SAO NAM - Đại lý & Trung tâm dịch vụ Particle Measuring Systems tại Việt Nam




_-02-01-2024-10-19-51.jpg)



_-02-01-2024-11-57-38.jpg)










_-27-12-2023-12-39-56.jpg)
.png)



