
Hướng Dẫn Chi Tiết về Phòng Sạch Theo Tiêu Chuẩn Quốc Tế - cho Ngành Dược
-
Hãng sản xuất: PMS - Mỹ Model: Document: -
Liên hệ
Hướng Dẫn Chi Tiết về Phòng Sạch Theo Tiêu Chuẩn Quốc Tế
Phân loại phòng sạch cho ứng dụng dược phẩm
Trong sản xuất dược phẩm, đặc biệt là thuốc vô trùng, vaccine, sinh phẩm, thuốc tiêm và các sản phẩm nhạy cảm, ô nhiễm từ hạt bụi, vi sinh vật, con người, thiết bị hoặc môi trường có thể ảnh hưởng trực tiếp đến chất lượng sản phẩm. Phòng sạch được thiết kế để giảm và kiểm soát các nguồn ô nhiễm này ở mức phù hợp với yêu cầu sản xuất.
Một phòng sạch đạt chuẩn không chỉ là phòng có tường, trần, sàn và bộ lọc HEPA. Phòng sạch phải là một hệ thống hoàn chỉnh gồm thiết kế, HVAC, luồng người, luồng vật liệu, quy trình vệ sinh, đào tạo nhân sự, giám sát môi trường, hiệu chuẩn thiết bị và dữ liệu chứng minh trạng thái kiểm soát.
Phòng sạch là khu vực được kiểm soát về số lượng hạt trong không khí, đồng thời có thể kiểm soát thêm nhiệt độ, độ ẩm, chênh áp, luồng khí và mức độ vi sinh tùy ứng dụng. Trong ngành dược phẩm, phòng sạch thường được sử dụng cho sản xuất, pha chế, chiết rót, đóng gói, kiểm nghiệm, bảo quản mẫu và các hoạt động cần hạn chế ô nhiễm.
ISO 14644 là bộ tiêu chuẩn quốc tế thường được sử dụng để phân loại phòng sạch dựa trên nồng độ hạt trong không khí. Khi phân loại phòng sạch, máy đếm tiểu phân sẽ được dùng để lấy mẫu tại các vị trí quy định, sau đó kết quả được so sánh với giới hạn của từng cấp sạch.
Trong ngành dược phẩm, ISO 14644 thường được dùng cùng với GMP, EU GMP Annex 1, PIC/S GMP và yêu cầu nội bộ của nhà máy. Điều quan trọng là phải hiểu rõ phòng sạch đang được đánh giá ở trạng thái nào: as-built, at-rest hay operational.
Trong dược phẩm, đặc biệt là sản xuất vô trùng, phòng sạch thường được quản lý theo cấp sạch GMP như Grade A, B, C và D. Mỗi cấp sạch có vai trò khác nhau trong dây chuyền sản xuất và yêu cầu kiểm soát khác nhau về tiểu phân, vi sinh, thao tác, trang phục, luồng khí và giám sát môi trường.
Phòng sạch hoạt động hiệu quả khi nhiều yếu tố được kiểm soát đồng bộ. Nếu chỉ đầu tư bộ lọc tốt nhưng vận hành sai, cửa mở liên tục, chênh áp không ổn định hoặc nhân sự thao tác chưa đúng, phòng sạch vẫn có thể phát sinh dữ liệu tiểu phân hoặc vi sinh bất thường.
Giám sát tiểu phân giúp nhà máy biết phòng sạch đang duy trì độ sạch như mong muốn hay không. Dữ liệu tiểu phân có thể được dùng cho phân loại phòng sạch, giám sát thường quy, đánh giá xu hướng, điều tra sai lệch, kiểm tra sau bảo trì và chứng minh trạng thái kiểm soát khi audit.
Dữ liệu tiểu phân cho biết độ sạch vật lý của không khí, nhưng không thể thay thế dữ liệu vi sinh. Trong dược phẩm, đặc biệt khu vô trùng, giám sát vi sinh giúp phát hiện nguy cơ nhiễm vi sinh từ không khí, bề mặt, nhân sự, thiết bị và thao tác sản xuất.
Phòng sạch cần được kiểm tra và thẩm định định kỳ để chứng minh vẫn đáp ứng yêu cầu thiết kế và yêu cầu GMP. Tùy mục tiêu, việc kiểm tra có thể bao gồm phân loại phòng sạch, kiểm tra rò rỉ HEPA, đo tốc độ gió, đo số lần trao đổi khí, kiểm tra chênh áp, smoke study, phục hồi phòng sạch và đánh giá dữ liệu giám sát.
SAO NAM hỗ trợ khách hàng tại Việt Nam trong các giải pháp thiết bị Particle Measuring Systems, giám sát tiểu phân, giám sát vi sinh, hiệu chuẩn, sửa chữa, bảo trì, cho thuê thiết bị và tư vấn hệ thống giám sát phòng sạch. Với khách hàng dược phẩm, việc quản lý đúng thiết bị và dữ liệu giúp tăng độ tin cậy khi vận hành GMP và chuẩn bị audit.
Pharmaceutical cleanrooms require proper classification, HVAC control, HEPA filtration, pressure cascade, particle monitoring, microbial monitoring, validation, calibration and GMP documentation. Cleanroom performance should be demonstrated by reliable data and risk-based environmental monitoring.
SAO NAM supports customers in Vietnam with Particle Measuring Systems equipment, cleanroom particle counters, microbial air samplers, online monitoring systems, calibration, maintenance, repair and technical consultation for GMP cleanroom applications.
For cleanroom monitoring, PMS equipment calibration, particle counting, microbial monitoring or pre-audit equipment readiness support, please contact SAO NAM via hotline, Zalo or email.
Thẩm định phòng sạch dược phẩm
Đếm hạt tiểu phân trong phòng sạch dược phẩm
Giám sát tiểu phân phòng sạch
Giám sát vi sinh vật trong môi trường phòng sạch
Tiêu chí lựa chọn máy lấy mẫu vi sinh theo ISO 14698
Lasair Pro - Máy đếm tiểu phân trong không khí
Airnet 510 - Sensor đếm tiểu phân online
IsoAir Pro-E - Máy đếm tiểu phân online
MiniCapt Remote - Máy lấy mẫu vi sinh online
Pharmaceutical Net Pro - Phần mềm giám sát tiểu phân và vi sinh
Hiệu chuẩn thiết bị Particle Measuring Systems
Sửa chữa thiết bị PMS
Cho thuê máy đếm tiểu phân phòng sạch

Các sản phẩm dược phẩm được sản xuất để đáp ứng các tiêu chuẩn khắt khe về hiệu quả và chất lượng. Mọi khía cạnh của chất lượng đều được xem xét, cân nhắc các rủi ro liên quan đến phương pháp giao hàng (tiêm, uống, v.v.) và cách thức sản xuất (vô trùng, tiệt trùng cuối cùng, hoặc dưới điều kiện kiểm soát kém hơn).
Bài viết này nghiên cứu hai phần của quá trình đó: chất lượng môi trường nơi sản phẩm được sản xuất và các tiêu chuẩn xung quanh giới hạn nồng độ hạt xác định những gì một môi trường kiểm soát bao gồm.
Bài viết này xét các tiêu chuẩn cho kiểm tra vật lý (EN ISO 14644-1:2015 [1]) và các tiêu chuẩn áp dụng trong hướng dẫn quy định (EU GMP Phụ lục 1 [2]).
ISO 14644-1 Vào năm 1999, bộ tiêu chuẩn phân loại phòng sạch mới ISO 14644 được kích hoạt, đầu tiên là ISO 14644-1, xác định phương pháp mà một phòng được phân loại và số lượng hạt tối đa cho phép trong một thể tích không khí cố định. Người đọc nên lưu ý rằng mặc dù ISO 14644 đã được áp dụng toàn cầu cho phân loại phòng sạch, có sự khác biệt cho việc giám sát thường xuyên, đặc biệt là giữa ISO 14644 và EU và WHO GMP.
Trạng thái chứng nhận của phòng sạch phải được xác định trước khi kiểm tra; ba trạng thái tồn tại trong bối cảnh của ISO 14644-1:
- As Built: phòng hoàn thành với tất cả các dịch vụ được kết nối và hoạt động nhưng không có thiết bị sản xuất hay nhân viên trong cơ sở.
- At Rest: tất cả các dịch vụ được kết nối, tất cả các thiết bị được lắp đặt và hoạt động theo cách thức đã được thỏa thuận, nhưng không có nhân viên hiện diện.
- Operational: tất cả thiết bị được lắp đặt và hoạt động theo định dạng đã được thỏa thuận và một số lượng nhân viên được xác định có mặt, làm việc theo một quy trình đã được thỏa thuận.
Giới hạn cho nồng độ phòng sạch của hạt lớn hơn một kích thước được quy định được xác định và trình bày trong Bảng 1 (dưới đây).
Bảng 1: Các lớp sạch hạt không khí cho phòng sạch và khu vực sạch (như được chỉ ra trong ISO 14644)
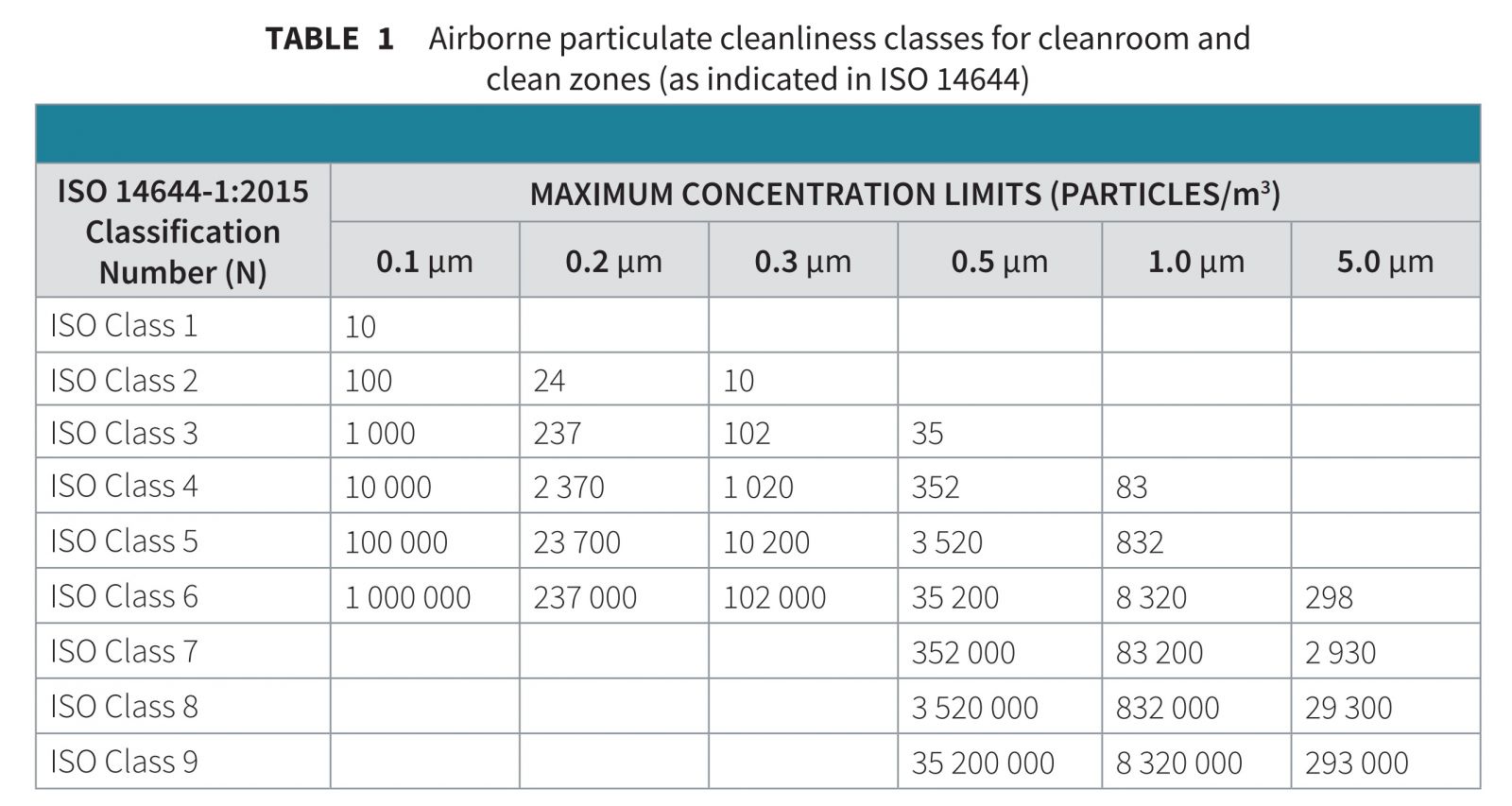
| Lớp Phân Loại ISO | Giới Hạn Nồng Độ Tối Đa (Hạt/m³) |
|---|---|
| 0.1 µm | 0.2 µm |
| Lớp 1 ISO | 10 |
| Lớp 2 ISO | 100 |
| Lớp 3 ISO | 1,000 |
| Lớp 4 ISO | 10,000 |
| Lớp 5 ISO | 100,000 |
| Lớp 6 ISO | 1,000,000 |
| Lớp 7 ISO | 352,000 |
| Lớp 8 ISO | 3,520,000 |
| Lớp 9 ISO | 35,200,000 |
Các giới hạn này đã được xác định theo tính toán từ tiêu chuẩn sử dụng công thức cho các lớp thập phân trung gian:
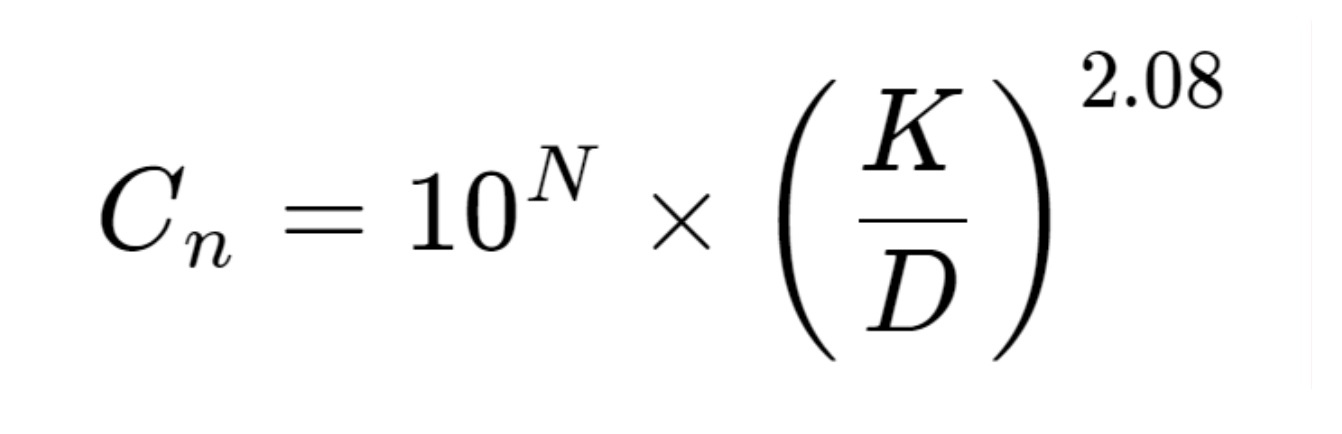
Trong đó:
- Cn: là nồng độ tối đa cho phép (hạt trên mỗi mét khối) của các hạt không khí bằng hoặc lớn hơn kích thước hạt được xem xét.
- N: là số lớp phân loại ISO, không được vượt quá giá trị 9 hoặc nhỏ hơn 1.
- D: là kích thước hạt được xem xét, tính bằng micromet, không được liệt kê trong Bảng E-1.
- K: là một hằng số, 0.1, biểu thị bằng micromet.
Do đó, mối quan hệ giữa kích thước hạt và sự phong phú của nó trong một quần thể là một chức năng của (1/D) 2.08 , và nếu kích thước hạt được vẽ trên một biểu đồ log/log với nồng độ của nó, độ dốc của đường cong cho mỗi lớp là 2.08; mối quan hệ này được hiển thị trong bảng trên.
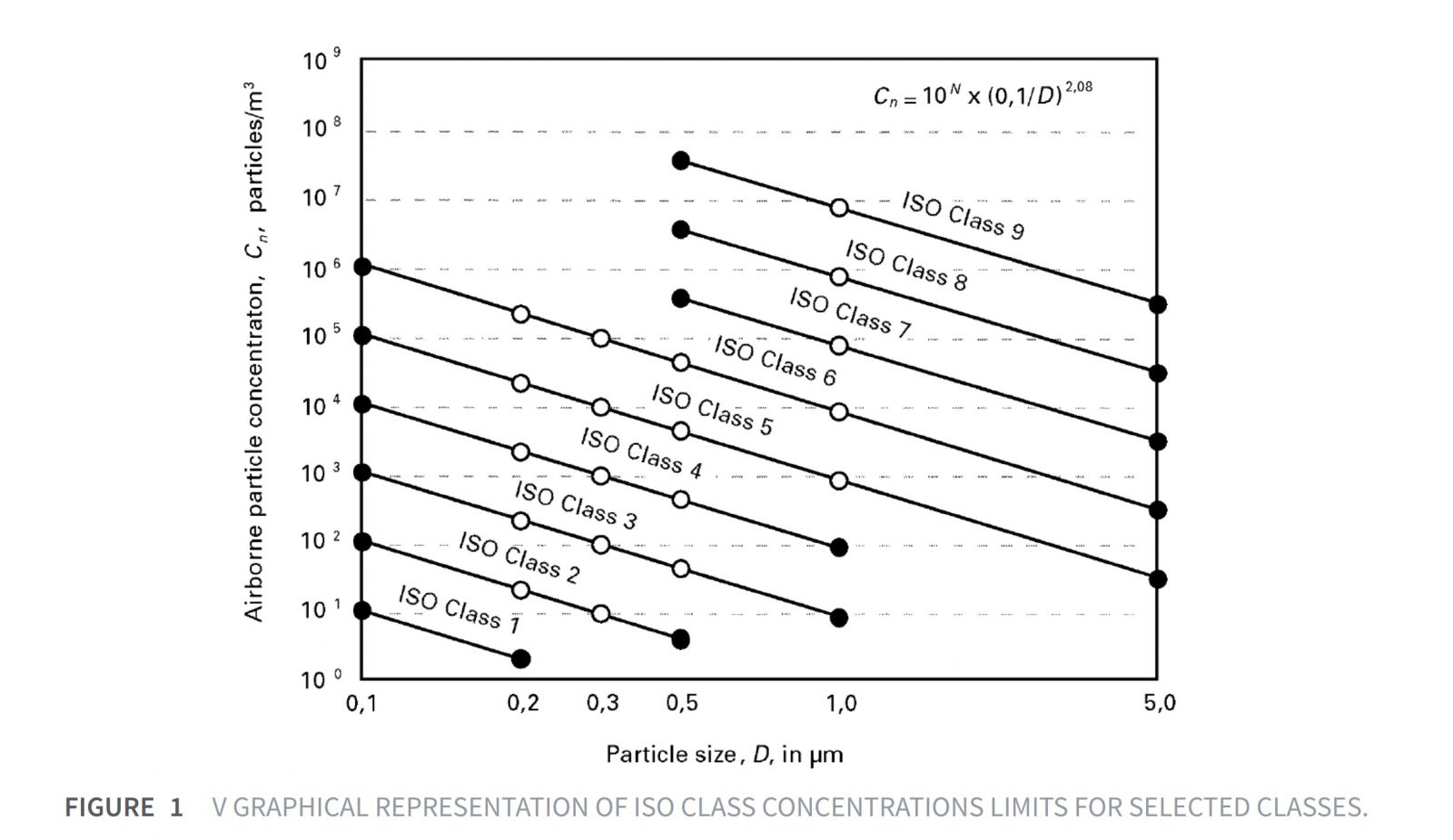
Hình 1V: Biểu Đồ Biểu Diễn Giới Hạn Nồng Độ Hạt ISO cho Các Lớp Được Chọn.
Việc chỉ định chứng nhận cho phòng sạch hoặc khu vực sạch cũng cần bao gồm các yếu tố sau:
- Số lớp phân loại của phòng được biểu thị là "Lớp ISO N".
- Trạng thái sử dụng của phòng.
- Kích thước hạt được xem xét. Cũng có thể chứng nhận phòng sạch ở nhiều kích thước khác nhau; nếu trường hợp này xảy ra thì yêu cầu về khối lượng mẫu cho kích thước hạt lớn nhất sẽ được sử dụng.
Ví dụ: Một thiết bị dòng chảy không khí đơn hướng x là khu vực sạch lớp ISO 5 tại 0.5 µm (3520 hạt/m³) trong trạng thái hoạt động.
Khu vực sạch này bây giờ cần được kiểm tra để chứng minh những phát biểu trên; tiêu chuẩn ISO 14644-1 xác định từng bước thành phần cần thiết để chứng minh sự tuân thủ.
Giả sử chúng ta có một thiết bị làm sạch không khí mà chúng ta muốn sử dụng cho khu vực chuẩn bị aseptic. Khu vực này cần đáp ứng Lớp ISO 5 tại 0.5 µm (≡ 10,000 hạt/ft³) trong trạng thái hoạt động, làm thế nào để chúng ta tiến hành xác định phân loại cho khu vực này?
Phòng có kích thước 12 m x 5 m (60 m²) và có một bàn làm việc ở trung tâm phòng.
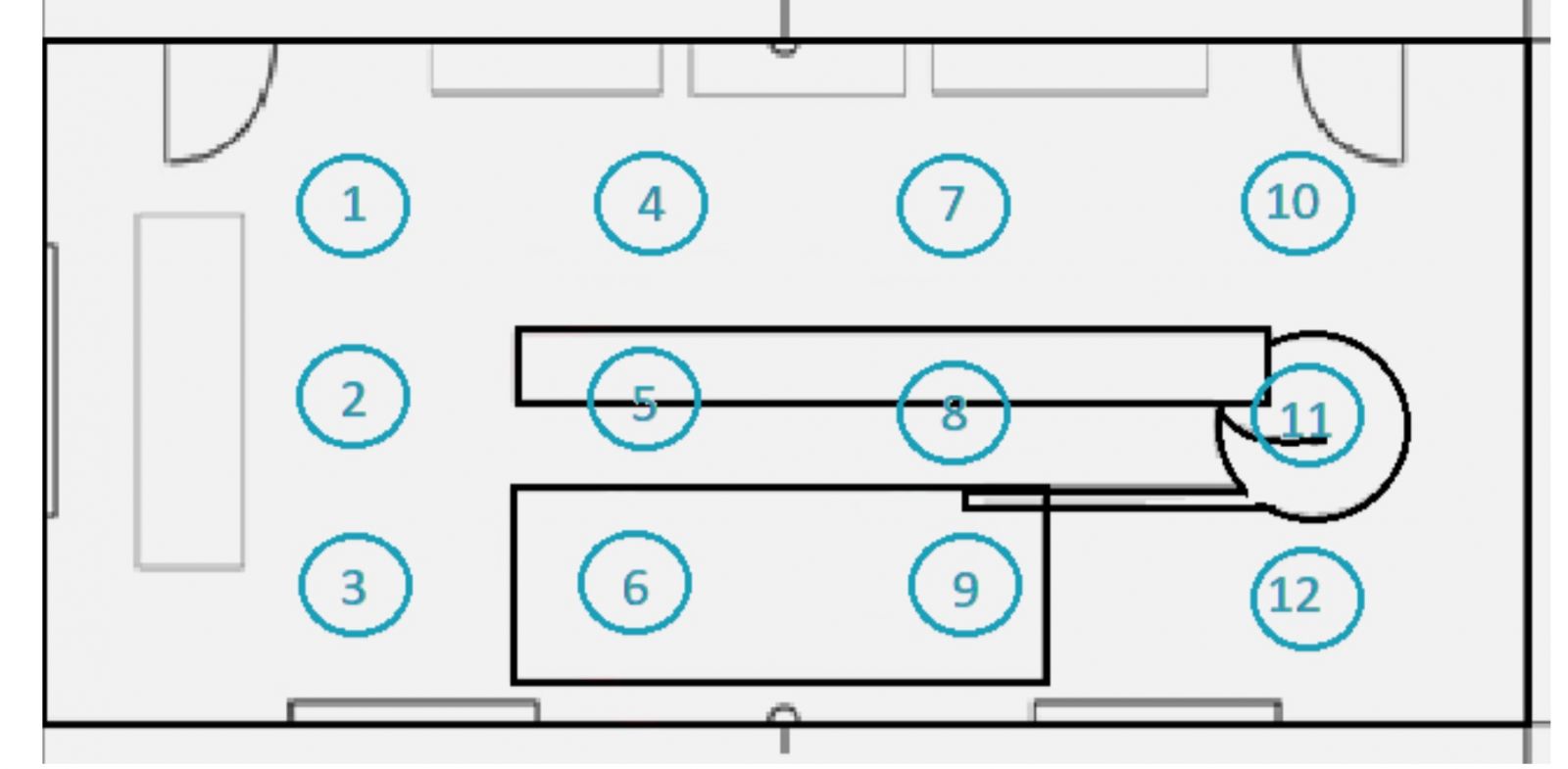
Hình 2: Sơ đồ cho thấy các vị trí phân loại trong khu vực sạch
Bước 1. Tính toán nồng độ hạt tối đa cho phép

- Hình 3. Tính toán nồng độ hạt tối đa cho phép
- Nồng độ tối đa cho phép là 3520 hạt/m³.
- Số lớp ISO là 5.
- Kích thước hạt được xem xét là 0.5 µm.
- Hằng số là 0.1 µm, được biểu thị là 0.1 µm.
Bước 2. Xác định số lượng vị trí lấy mẫu từ bảng dưới đây
- Bảng 2. Số lượng vị trí lấy mẫu cần thiết
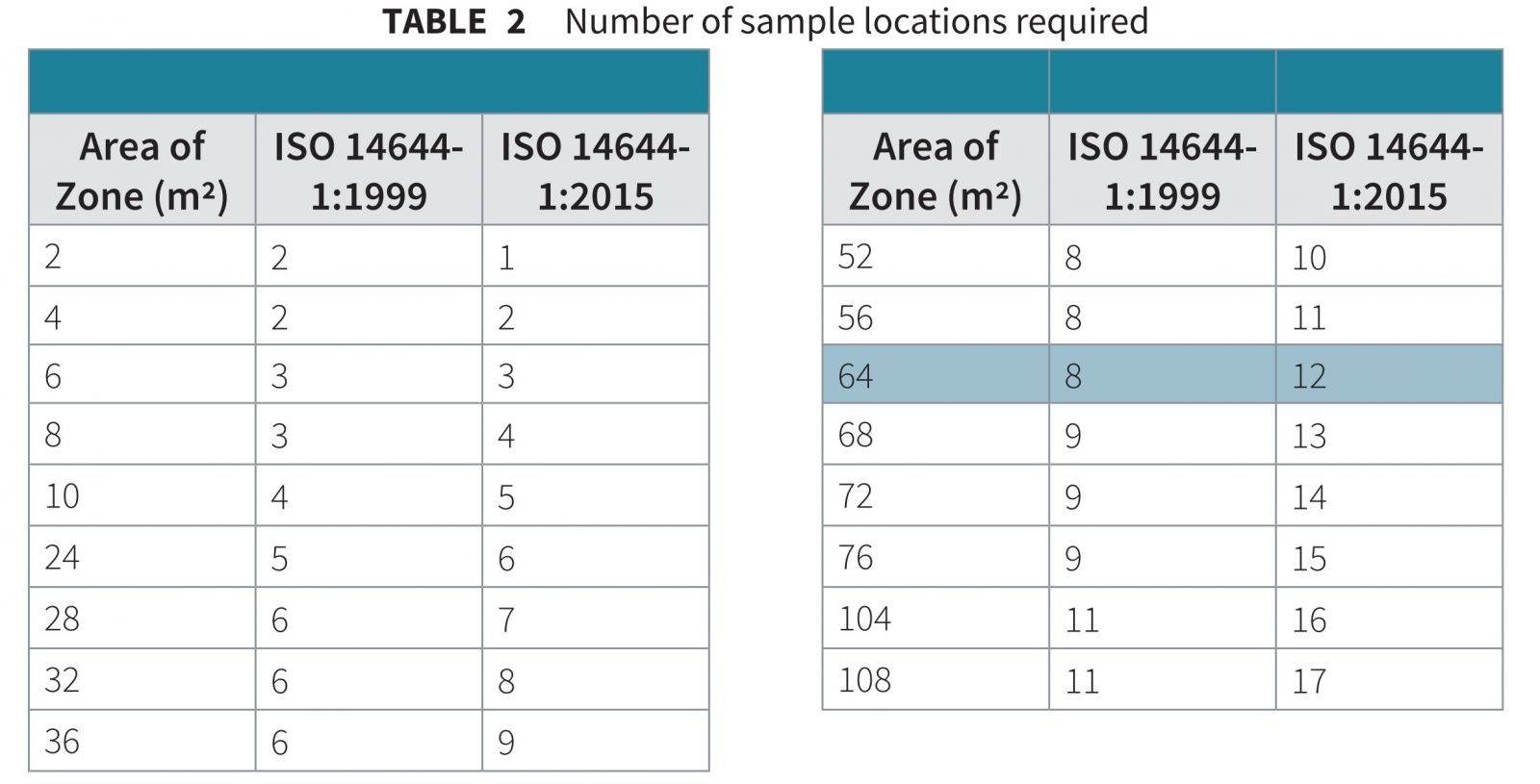
Bước 3. Tính toán thể tích mẫu
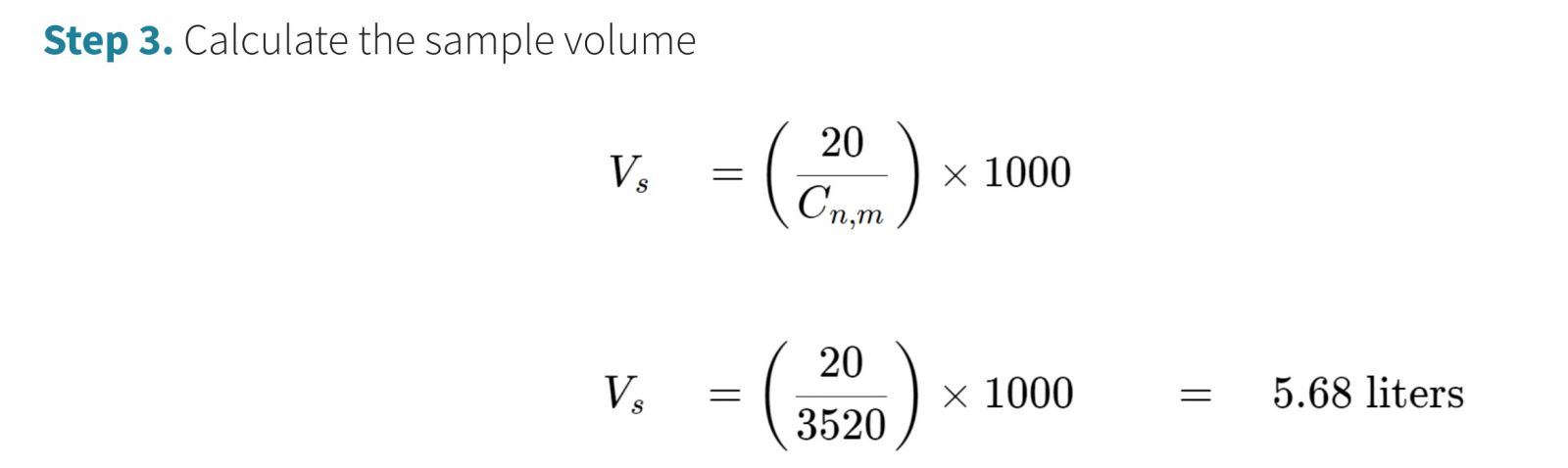
- Theo ISO 14644-1:2015, công thức này tìm thể tích mẫu là 5.68 lít. Đối với một máy đếm hạt tiêu chuẩn có lưu lượng 28.3 L/phút, một mẫu trong 1 phút sẽ vượt qua tiêu chuẩn thể tích mẫu tối thiểu.
Vì vậy, để đáp ứng thông số kỹ thuật, chúng ta sẽ lấy một mẫu 1 phút tại mỗi trong 12 vị trí.
Bước 4. Thực hiện đo lường tại mỗi vị trí (1 phút mỗi mẫu) và ghi lại kết quả
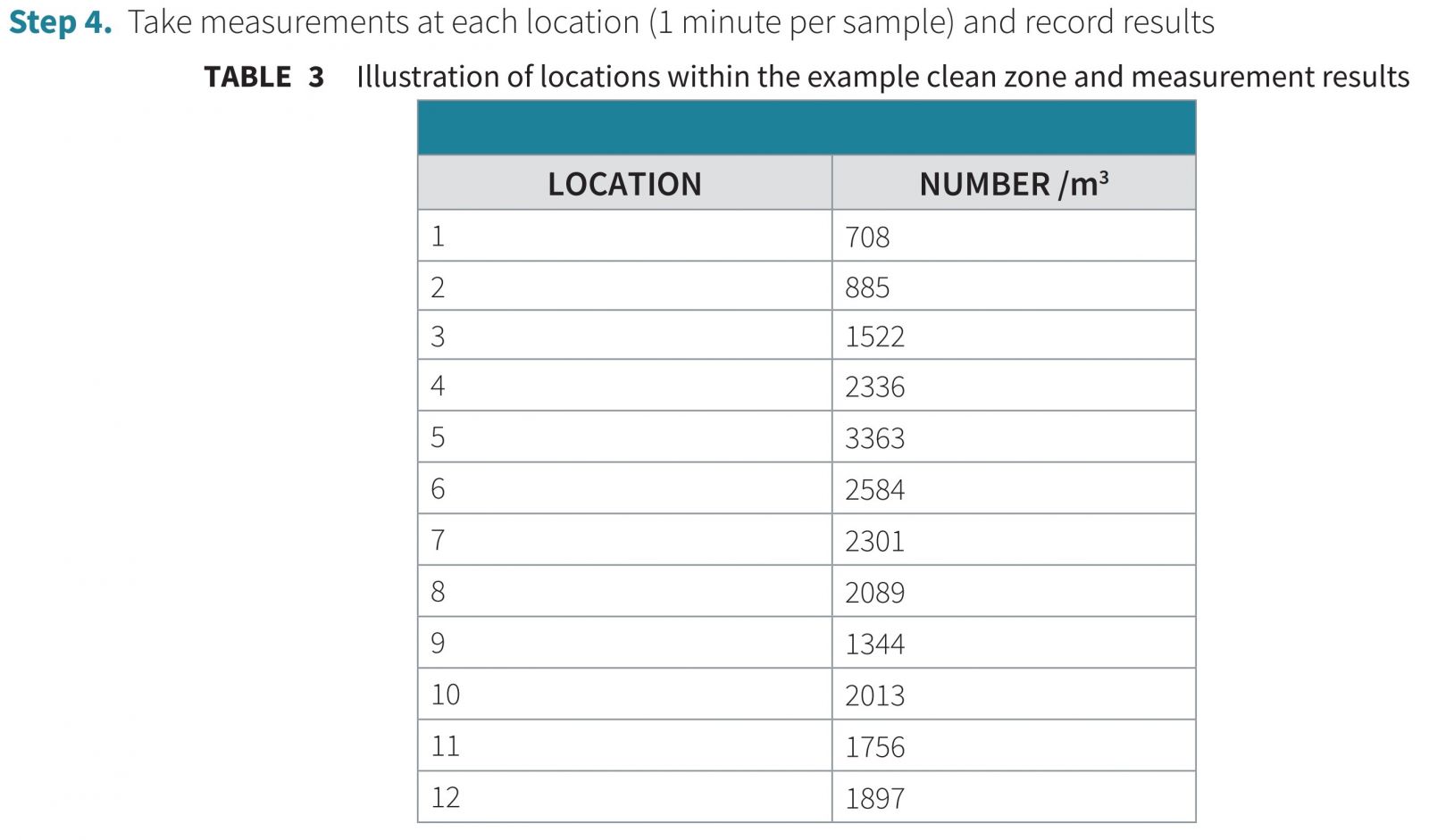
- Bảng 3. Minh họa các vị trí trong khu vực sạch mẫu và kết quả đo lường
Bước 5. Lập báo cáo
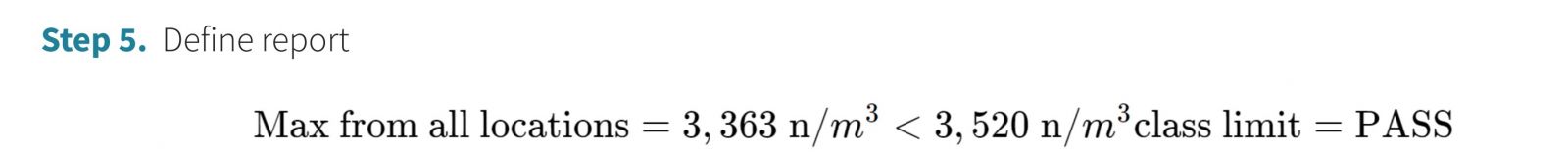
- Khu vực này đáp ứng thông số kỹ thuật cho khu vực sạch lớp ISO 5 tại 0.5 µm và bây giờ có thể được sử dụng cho mục đích mà nó được thiết kế. Phân loại phòng sẽ cần được lặp lại theo tần suất được xác định bởi ISO 14644-2 [3].
Phụ lục 1 GMP của EU
- Hướng dẫn GMP của Liên minh Châu Âu cho sản xuất vô trùng đã được sửa đổi vào năm 2003 để thích ứng với các thay đổi từ các tiêu chuẩn phòng sạch khác nhau thành một tiêu chuẩn phòng sạch thống nhất, ISO4644-1. Trang đầu tiên ghi nhận điều này:
- “Phụ lục 1 của Hướng dẫn Thực hành Sản xuất Tốt EC (GMP) cung cấp hướng dẫn bổ sung về việc áp dụng các nguyên tắc và hướng dẫn của GMP cho các sản phẩm dược liệu vô trùng. Hướng dẫn bao gồm các khuyến nghị về tiêu chuẩn vệ sinh môi trường cho phòng sạch. Hướng dẫn đã được xem xét lại theo tiêu chuẩn quốc tế EN/ISO 14644-1 và được sửa đổi nhằm mục đích hài hòa nhưng vẫn tính đến những mối quan tâm đặc biệt đối với sản xuất các sản phẩm dược liệu vô trùng.”
- Cụ thể, phương thức mà một phòng sạch được chứng nhận cần phải tuân thủ các quy tắc và định dạng của hướng dẫn ISO14644-1, nhưng, tiêu chuẩn ISO đã được điều chỉnh liên quan đến các sản phẩm dược liệu vô trùng. Để mục đích này, một bảng giá trị chứng nhận phòng sạch tương đối tương đương với ISO 14644-1 đã được xác định.
Để rõ ràng, một loạt các ghi chú được thêm vào bảng, thật không may, ghi chú đầu tiên, Ghi chú ‘a’, đã gây ra một số nhầm lẫn. Sự nhầm lẫn này đã được giải quyết trong bản phát hành Phụ lục 1 GMP của EU năm 2008, trong đó mô tả rõ ràng ba giai đoạn.
Các hoạt động cần thực hiện được liệt kê như sau [5]. Đầu tiên, mỗi phòng sạch và thiết bị không khí sạch cần được phân loại; sau đó, chúng cần được giám sát để xác minh rằng điều kiện đang được duy trì phù hợp với chất lượng sản phẩm và dữ liệu thu thập từ quá trình giám sát này cần được xem xét trong bối cảnh rủi ro đối với chất lượng sản phẩm hoàn thiện.
Bảng 4 EU GMP Phụ lục 1:2008 phân loại phòng
Người đọc sẽ lưu ý, như đã chỉ ra ở trên, rằng các giới hạn trong bảng GMP của EU có sự khác biệt nhẹ so với tiêu chuẩn ISO 14644. Để thực hiện chứng nhận cần thiết, điều quan trọng là phải hiểu cách thức hoạt động của ISO 14644-1, cách chứng nhận một phòng sạch theo tiêu chuẩn đó, các quy tắc về số điểm lấy mẫu, quy tắc về vị trí điểm lấy mẫu, quy tắc về thể tích mẫu cần lấy tại mỗi vị trí, và các quy tắc về phân tích thống kê dữ liệu phòng sạch cần được tuân thủ. Tuy nhiên, thay vì sử dụng bảng phân loại giới hạn được quy định trong ISO 14644-1, người ta nên sử dụng bảng được in trong tài liệu hướng dẫn đã được sửa đổi.
Các kỳ vọng khác cũng được định nghĩa bởi GMP. Đây có thể là các kỳ vọng như có một khối lượng mẫu cho Cấp A là 1 m³ cho mỗi vị trí lấy mẫu hoặc sử dụng chiều dài ống lấy mẫu tối thiểu do sự kết tủa cao của hạt 5.0 µm trong ống truyền (lý tưởng là không nên sử dụng ống lấy mẫu). Ngoài ra, việc chứng nhận lại phòng sạch nên theo hướng dẫn được đưa ra trong ISO 14644-2: một lần một năm cho Cấp ISO 6 trở lên và một lần sáu tháng cho Cấp ISO 5. Các ngoại lệ được thực hiện để mở rộng các khu vực Cấp ISO 5 nếu hệ thống giám sát liên tục đã được triển khai. Thời điểm thích hợp để thực hiện chứng nhận là các đợt đổ đầy truyền thông hoặc các đợt mô phỏng đổ đầy.
Phân loại phòng sạch theo GMP của EU
Trong đợt phát hành EU GMP Phụ lục 1 năm 2008, mọi sự nhầm lẫn đã được giải quyết rõ ràng, đặc biệt là ghi chú ‘a’ đã gây ra một số nhầm lẫn nhất định. Ghi chú này đã được sửa đổi trong phiên bản mới nhất của EU GMP Phụ lục 1, làm rõ ba giai đoạn cần thực hiện. Mỗi phòng sạch và thiết bị không khí sạch cần được phân loại trước; sau đó cần được giám sát để xác minh rằng điều kiện đang được duy trì phù hợp với chất lượng sản phẩm và dữ liệu thu được từ việc giám sát này cần được xem xét trong bối cảnh rủi ro đối với chất lượng sản phẩm hoàn thành.
Bảng 4 EU GMP Phụ lục 1:2008 bảng phân loại phòng
| Cấp độ GMP của EU | Tại Chỗ | Trong Quá Trình Hoạt Động |
|---|---|---|
Số lượng h
|
 SAO NAM - Đại lý & Trung tâm dịch vụ Particle Measuring Systems tại Việt Nam
SAO NAM - Đại lý & Trung tâm dịch vụ Particle Measuring Systems tại Việt Nam




_-02-01-2024-10-19-51.jpg)



_-02-01-2024-11-57-38.jpg)











_-27-12-2023-12-39-56.jpg)
.png)



